Die EU-Fälschungsschutzrichtlinie von Februar 2019 verpflichtet Hersteller, Packungen über individuelle Seriennummern im 2D-DataMatrix-Code zu serialisieren und mit Erstöffnungsschutz auszustatten. Diese Maßnahmen ermöglichen eine lückenlose Rückverfolgbarkeit und Echtheitsprüfung durch das European Medicines Verification System sowie über securPharm in Deutschland. b+b Automations- und Steuerungstechnik warnt vor unzureichender Datenqualität, empfiehlt Validierungsprozesse und stellt eine umfassende Checkliste zur Optimierung von Druck-, Verifikations- und Ausnahmeszenarien bereit, die automatisierte Chargen- und Verfallsdaten erfasst und Rückrufe vereinfacht.
Inhaltsverzeichnis: Das erwartet Sie in diesem Artikel
FMD bindet seit 2019 verbindlich gesamte legale Arzneimittellieferkette ein

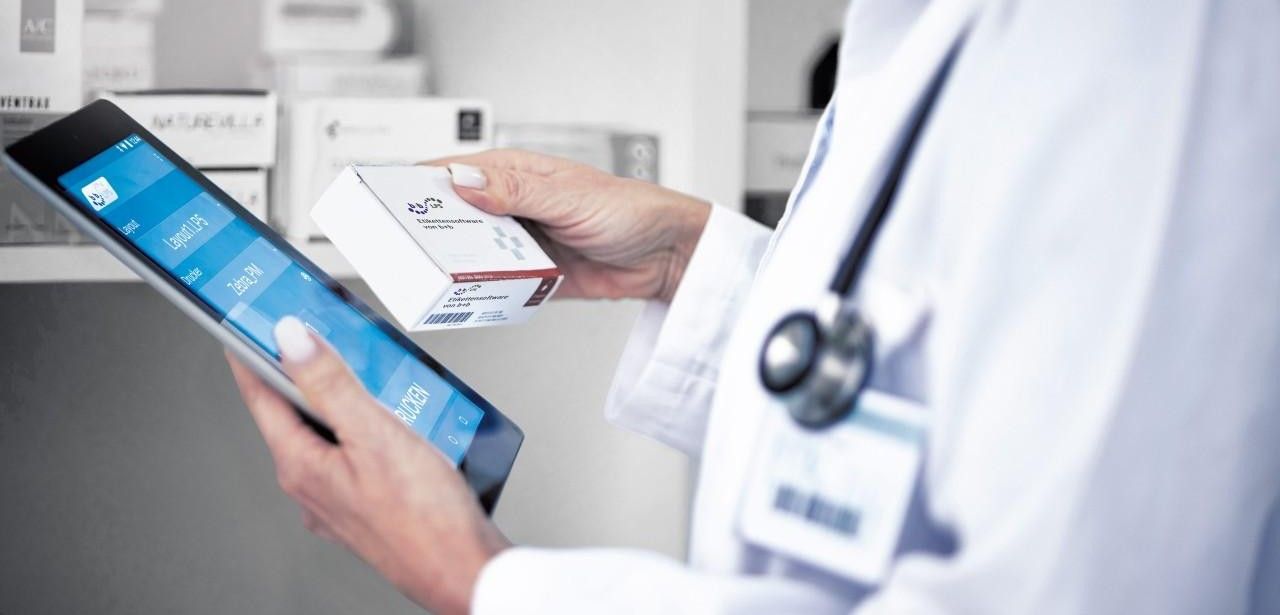
bb TE PV Pharmaserialisierung (Foto: b+b Automations- und Steuerungstechnik GmbH)
Gefälschte Medikamente bergen weitreichende gesundheitliche Gefahren, da sie inaktiven oder kontaminierten Wirkstoffen enthalten können, und sie untergraben das Vertrauen von Verbrauchern und Fachkräften in medizinische Systeme. Um die Authentizität der legalen Lieferkette sicherzustellen, verabschiedete die Europäische Union im Jahr 2011 die Falsified Medicines Directive (FMD). Seit Februar 2019 gilt diese Verordnung verbindlich und verpflichtet Hersteller wie Vertreiber zu Maßnahmen wie Serialisierung, Datenübermittlung und Erstöffnungsschutz sowie über europaweite Sicherheitsprozesse und transparent und lückenlos.
FMD-Sicherheitskonzept: Serialisierung garantiert vollständig eindeutige maschinelle Packungsidentifikation per DataMatrix-Code
Im Rahmen der EU-FMD-Richtlinie stellt die Serialisierung das Herzstück des Sicherheitskonzepts dar. Jede Arzneimittelpackung wird mit einer einzigartigen Seriennummer versehen, die in einem maschinenlesbaren 2D-DataMatrix-Code untergebracht ist und neben GTIN, Charge und Verfallsdatum alle relevanten Informationen enthält. Ein mechanischer Erstöffnungsschutz an der Verpackung signalisiert zuverlässig jede vorzeitige Öffnung, sodass Manipulationsversuche bereits vor Abgabe im Apotheken- oder Klinikbereich nachgewiesen werden können. Dieses integrierte Verfahren sichert Produktintegrität und erhöht Patientenvertrauen.
Verpflichtende DataMatrix-Daten sicherstellen eindeutige Identifikation und Rückverfolgung von Packungen
Jede Arzneimittelpackung wird mit einem DataMatrix-Code versehen, der zwingend den Produktcode (GTIN, NTIN oder PPN), die einmalige Seriennummer, Chargennummer und Verfallsdatum abbildet. Diese systematische Datenkomposition gewährleistet eine eindeutige Identifikation jeder Einheit und unterstützt die Rückverfolgbarkeit über alle Produktions- und Distributionsstufen hinweg. Automatisierte Prüfprozesse lesen die kodierten Informationen aus und ermöglichen eine schnelle Authentifizierung, während gleichzeitig Warenausfälle oder Fälschungen zuverlässig erkannt werden.
Unvollständige Datensätze lösen Störungen in Produktion und Logistik aus
Laute Einschätzung der b+b Automations- und Steuerungstechnik GmbH wird fortwährend betont, dass die Relevanz von qualitativ hochwertigen Daten in Serialisierungsabläufen vielfach unterschätzt wird. Unvollständige Datensätze lösen in Verifikationssystemen vermehrt Fehlermeldungen aus. Diese führen wiederum zu Störungen und Unterbrechungen in Montage-, Verpackungs- und Logistikprozessen. Daher empfiehlt das Unternehmen, automatisierte Plausibilitätsprüfungen und standardisierte Datenfreigabeprozesse einzuführen, um konsistente Abläufe und termingerechte Produktlieferungen sicherzustellen. Regelmäßig aktualisierte Datenprofile mit Eskalationspfaden senken Fehlalarme effektiv deutlich nachhaltig.
Zentraler Hub verarbeitet Serialisierungsdaten zur Echtheitsprüfung europaweit in Echtzeit
Mit dem European Medicines Verification System (EMVS) wurde ein europaweit einheitliches und systemübergreifendes Datenbanknetzwerk zur Absicherung und Rückverfolgung von Arzneimitteln implementiert. Serialisierungsdaten der Hersteller werden an einen zentralen Hub übertragen und dort gespeichert. Nationale Plattformen wie securPharm nutzen diese Datensätze, um bei der Abgabe in Apotheken und Kliniken in Echtzeit Authentizitätsprüfungen durchzuführen. Dadurch wird jede verpackte Einheit entlang der Lieferkette lückenlos verifiziert und der Fälschungsschutz auf allen Versorgungsebenen dynamisch gestärkt.
Inkonsequente Decommissioning-Prozesse behindern reibungslose Pharmalogistik im Alltag trotz Standardisierung
Nach Abschluss der technischen Implementierung treten im Alltag oft Prozesslücken auf. Unklare Regeln zur Ausschleusung führen zu Verifikationsfehlern oder Blockierungen von Packungen. Decommissioning-Maßnahmen werden uneinheitlich umgesetzt, sodass abgemeldete Einheiten im System verbleiben. Ein fehlender Informationsabgleich zwischen Labeldruck, Echtheitsprüfung und Datenhaltung verzögert Abläufe. Außerdem wird die Aggregationsdatenerfassung nicht vollständig genutzt, weshalb Rückverfolgung, Reportings und Risikomanagement leiden. Diese Defizite beeinträchtigen Effizienz, Compliance und Resilienz nachhaltig. Standardisierung, Schulung und Monitoring reduzieren Risiken erheblich.
Praxisorientierte Checkliste von b+b identifiziert Risiken Druck und Verifizierung
Mit der praxisorientierten Checkliste von b+b lassen sich zentrale Risiken entlang der Serialisierung und Verifikation frühzeitig identifizieren und minimieren. Der Leitfaden deckt umfassend Druckprozesse mit Soll-Ist-Prüfungen, Verifizierungsabläufe gemäß EMVS-Anforderungen, systematisches Datenmanagement sowie die Anbindung an das European Medicines Verification System ab. Ergänzend berücksichtigt die Checkliste kritische Sonderprozesse wie Exportabwicklung, Retourenlogistik und Lohnverpackung, um eine rechtssichere, effiziente und auditfeste Supply-Chain-Gestaltung sicherzustellen. Sie bietet klare Handlungsempfehlungen, Prozesskennzahlen sowie Verantwortungszuweisungen für beteiligte Stakeholder.
Serialisierung steigert Transparenz, ermöglicht Rückrufe und optimiert Vertriebswege effizient
Die Einführung einer flächendeckenden Serialisierung erlaubt die automatische Erfassung von Chargen- und Ablaufdaten in Echtzeit, wodurch die Präzision bei Lagerbestandsprüfungen wesentlich erhöht wird. Rückrufaktionen lassen sich gezielt und schnell durchführen, da Daten sofort verfügbar sind. Durch diese transparente Datengrundlage werden Durchlaufzeiten nachvollziehbar gemessen und Engpässe frühzeitig erkannt. Zusätzlich ermöglichen umfassende Vertriebsanalysen eine Optimierung von Distributionswegen und liefern wertvolle Impulse für Prozessverbesserungen, die Effizienz steigern und Betriebskosten senken nachhaltig sichtbar quantifizierbar.
Serialisierung wird strategischer Baustein moderner Pharma-Logistik für mehr Sicherheit
Zukunftsweisende Track-and-Trace-Lösungen digitalisieren sämtliche Teilschritte innerhalb der Arzneimittellogistik. Durch die paritätische Erfassung aller Umschlagspunkte und Lagerstationen entsteht eine durchgängige Transparenz entlang der gesamten Lieferkette. Dieses Paradigma macht die Serialisierung zum strategischen Kernstück moderner Supply-Chain-Managements im Pharmabereich, indem Produktechtheit konsequent geprüft, Schwachstellen schnell identifiziert und Effizienzpotenziale optimal ausgeschöpft werden. Echtzeitmonitoring minimiert Ausfallzeiten, während automatische Validierungen regulatorische Anforderungen nachhaltig unterstützen und vertrauenswürdige Abläufe gewährleisten.
Präzise Daten und Echtzeit-Verifikation steigern Compliance, Schutz und Logistikeffizienz
Mit der verbindlichen Umsetzung der EU-FMD-Serialisierung erzielen Hersteller und Lohnverpacker eine deutlich höhere Arzneimittelsicherheit, da jede Packung über einen eindeutigen DataMatrix-Code verfügt. Durch lückenlose Datenaufzeichnung, Echtzeitverifikation und standardisierte Checklisten lassen sich Prozessrisiken minimieren und Rückrufe zielgenau steuern. Gleichzeitig verbessern sich Compliance-Werte und Transparenz innerhalb der Lieferkette. Die umfassende Datenerfassung bietet darüber hinaus Grundlagen für Effizienzsteigerungen und nachhaltige Optimierungen in der modernen Pharma-Logistik unter Einsatz innovativer digitaler Qualitätssicherungsmaßnahmen und lückenloser Auditfähigkeit.